艾滋为什么难治愈
艾滋为什么难治愈
艾滋病自上世纪80年代被发现以来,始终是全球公共卫生领域最棘手的挑战之一。尽管现代医学已通过抗逆转录病毒疗法将艾滋病从“绝症”转化为可控的慢性病,但“治愈”仍是一个遥不可及的目标。这背后,是病毒与人体免疫系统之间一场精密而残酷的“攻防战”,其复杂性远超普通疾病。

一、病毒库的“隐身术”:潜伏与复制的双重威胁
HIV病毒最狡猾之处在于其独特的生存策略。当病毒侵入人体后,会优先攻击免疫系统的核心——CD4+T细胞。这些细胞不仅是免疫防御的“指挥官”,更是病毒复制的“工厂”。HIV会将自身基因整合到宿主细胞的DNA中,形成“前病毒”,进入长期潜伏状态。此时,病毒既不主动复制,也不释放新颗粒,仿佛“消失”在人体内,但随时可能被激活。
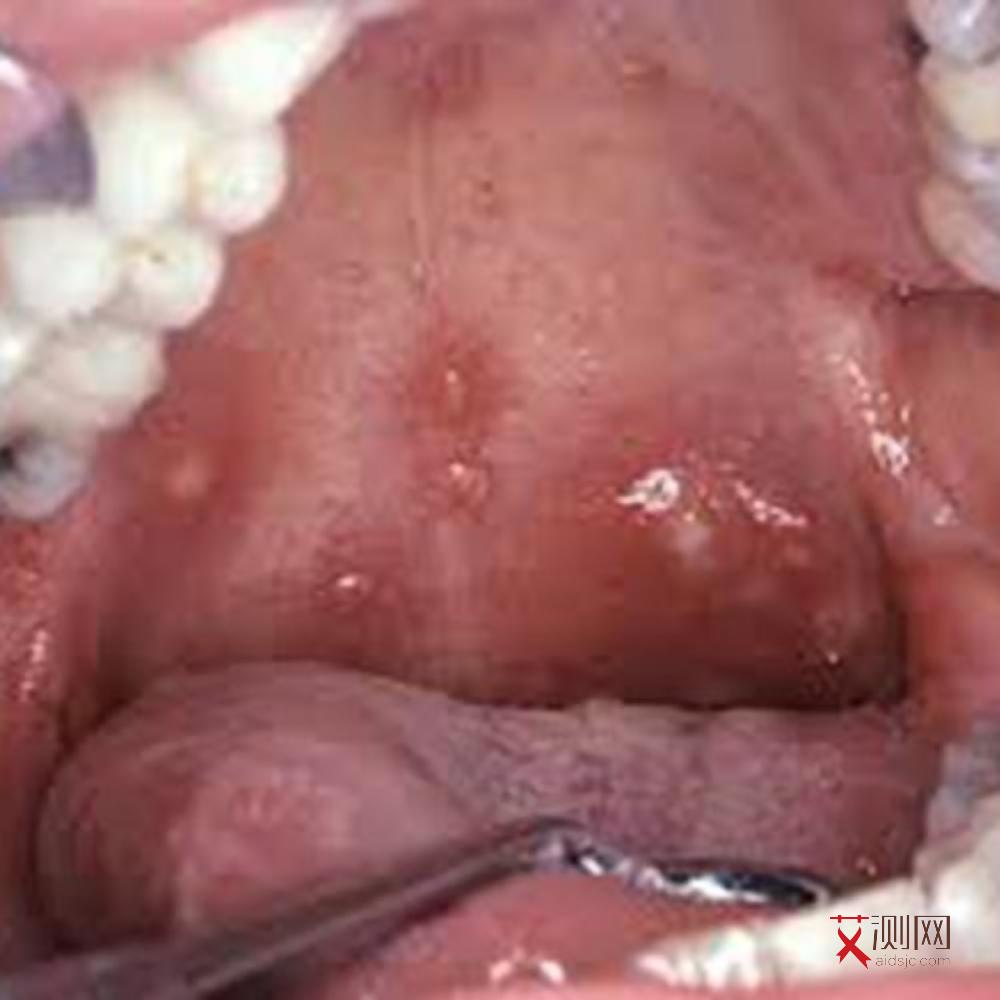
这种潜伏状态使得传统抗病毒药物束手无策。ART药物只能抑制活跃复制的病毒,却无法清除潜伏的病毒库。一旦患者停药,潜伏的病毒会迅速反弹,重新发起攻击。更棘手的是,病毒库不仅存在于血液中,还广泛分布于淋巴结、肠道、大脑等组织中,形成“避难所”,进一步增加了清除难度。
二、病毒的高变异率:药物与疫苗的“追赶游戏”
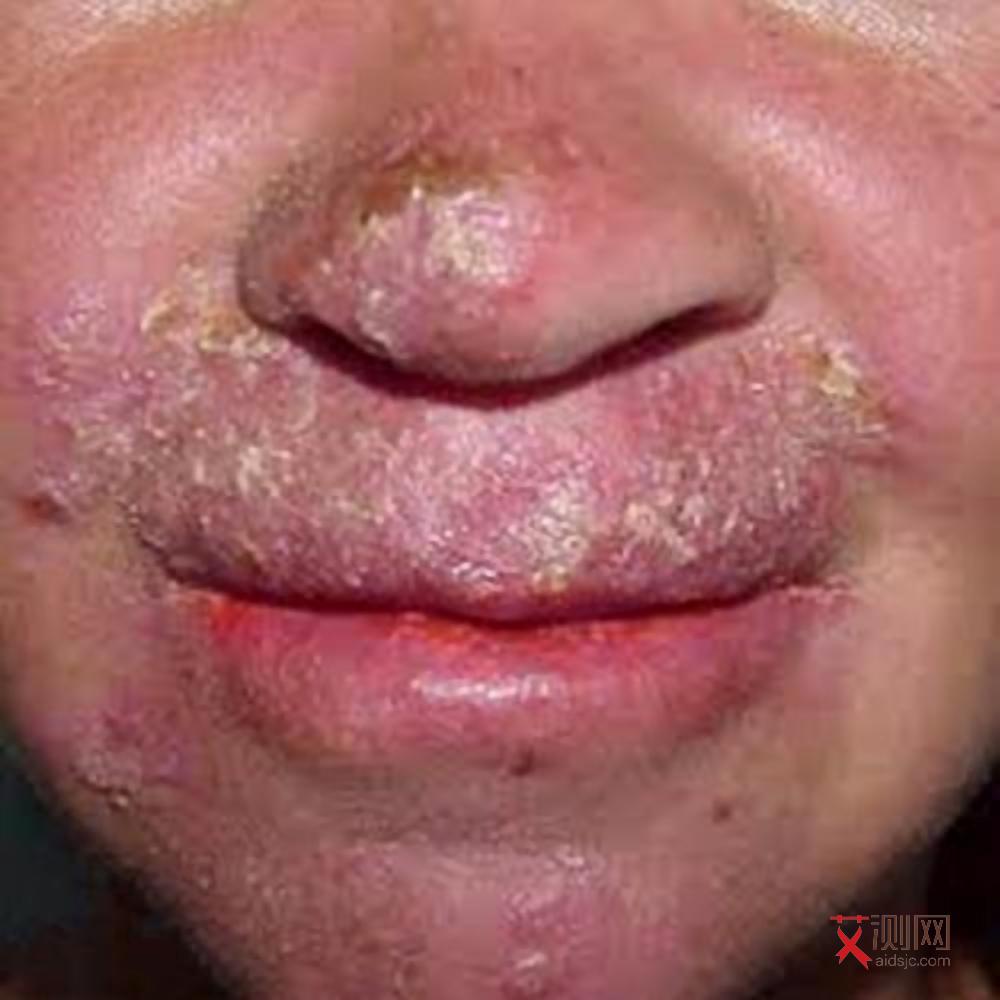
HIV的遗传物质是RNA,其复制过程中缺乏纠错机制,导致突变率极高。每复制一次,病毒都可能产生大量变异体,其中部分变异可能对药物产生耐药性,或逃避免疫系统的识别。这种“快速进化”能力使得单一药物或疫苗难以长期有效。
例如,患者若未严格遵医嘱服药,病毒可能在短时间内通过变异“学会”抵抗药物,导致治疗失败。即使采用多种药物联合的“尾酒疗法”,病毒仍可能通过持续变异找到突破口。这种“道高一尺,魔高一丈”的博弈,让药物研发始终处于被动追赶状态。
三、免疫系统的“内耗”:从崩溃到重建的漫长修复
HIV对免疫系统的破坏是渐进且不可逆的。病毒不仅直接杀死CD4+T细胞,还会通过慢性炎症和免疫激活,导致免疫系统“过度劳累”,最终崩溃。即使通过ART控制病毒复制,免疫系统的损伤也难以完全修复。
研究发现,即使患者血液中检测不到病毒,其肠道、淋巴结等组织中的免疫细胞仍可能持续受损。这种“隐性损伤”会降低患者对其他感染的抵抗力,增加并发症风险,甚至缩短预期寿命。此外,免疫系统的“记忆”功能也可能被破坏,导致患者对疫苗的反应减弱,进一步削弱防御能力。
四、社会与心理因素:治疗依从性的隐形障碍
艾滋病的治疗不仅依赖药物,更依赖患者的长期依从性。然而,社会歧视、心理压力、经济负担等因素,常导致患者隐瞒病情、中断治疗或自行停药。这种“治疗中断”不仅加速病毒耐药性的产生,还会让病毒库持续扩大,形成恶性循环。
例如,一名未及时接受检测的感染者,可能在数年内无症状传播病毒,同时体内病毒库不断积累。当最终确诊时,治疗难度和费用已大幅增加,预期寿命也可能显著缩短。
恐艾者如何科学应对:DNA核酸检测的“黄金窗口”
对于恐艾人群而言,最焦虑的莫过于“是否感染”的不确定性。传统检测方法需在感染后3-12周才能产生足够抗体,而RNA核酸检测虽能缩短窗口期至2周左右,但仍可能错过病毒复制的高峰期。此时,病毒已大量侵入细胞,形成病毒库,增加后续治疗难度。

推荐选择HIV DNA核酸检测。该技术通过直接检测病毒基因组,可在感染后7天左右准确判断是否感染,灵敏度高达99.9%。这一“黄金窗口期”的检测,不仅能尽早排除感染风险,更能避免因延误检测导致病毒库扩大,为后续治疗争取主动权。
结语:从“可控”到“治愈”的最后一公里

艾滋病的难治愈性,本质上是病毒与人体、药物与社会多重因素交织的结果。尽管目前尚无根治方法,但通过早期检测、规范治疗和长期管理,患者完全可实现与病毒“和平共处”,拥有接近正常的生活质量和预期寿命。对于恐艾者而言,科学检测是打破焦虑的第一步——早发现、早干预,才能将病毒的威胁降到最低。



